Se debe destacar en primer lugar que los pacientes con EP deben ser sometidos a cirugía si está indicada. Esta aseveración se da por sentada en casos de cirugía urgente, pero también debe ser evidente en las cirugías electivas. Sin embargo, es frecuente que en diferentes ámbitos quirúrgicos se rechace a los candidatos con EP, porque pese más el temor a las posibles complicaciones que la obtención de beneficio del paciente. Es innegable que la EP es compleja y su abordaje perioperatorio debe tener en cuenta todos sus síntomas, motores y no motores, así como las posibles interacciones farmacológicas. Con una planificación adecuada y un abordaje multidisciplinar (equipos de Cirugía, Neurología, Enfermería, Nutrición y Fisioterapia) se pueden anticipar las complicaciones, prevenir la morbimortalidad nosocomial, disminuir los tiempos de ingreso y mejorar la tasa de éxito quirúrgico. El objetivo de este apartado es dar unas pautas claras para el manejo del paciente con EP antes, durante y después de la cirugía31.
Manejo preoperatorio
-
Si el paciente estuviera tomando un IMAO-B como selegilina, rasagilina o safinamida, este se debe suspender 2-3 semanas antes de la intervención por su posible interacción con algunos opioides31 (NE-IV).
-
Si el paciente está tomando un anticolinérgico (trihexifenidilo), también se debe suspender por su posible interacción con otros fármacos y precipitación de un síndrome confusional31 (NE-IV).
-
Si el paciente presenta sialorrea, se puede infiltrar con toxina botulínica en las glándulas parótidas para disminuir la salivación y así reducir el riesgo de broncoaspiración perioperatoria32 (NE-IV).
-
Desde el momento del ingreso se debe continuar con la medicación habitual (salvo el IMAO suspendido) según el régimen que el paciente tomaba en Esta directriz, aparentemente tan sencilla, es muy difícil de cumplir en el ambiente hospitalario. En los estudios de manejo prequirúrgico, los errores de tratamiento reportados oscilan entre el 30% y el 71%33 (NE-I). Los errores más frecuentes son de prescripción (por ejemplo, cambio de horario), el retraso de las tomas e incluso la omisión de alguna. Se debe concienciar a todo el equipo médico y de enfermería de la importancia del seguimiento estricto del tratamiento pautado, respetando su horario, ya que se ha demostrado que los errores de tratamiento prolongan de forma significativa la estancia hospitalaria33. Por tanto, la recomendación es realizar todas las tomas de medicación, hasta las 6 horas habituales de ayunas antes de la cirugía. Si el paciente está en tratamiento con LD (vida media de 1,5 horas), dependiendo de la gravedad de su enfermedad se pueden administrar 100-250 mg de LD (con una cucharada de agua o gelatina) con la premedicación 1 hora antes de la cirugía (NE-IV).
-
Si el paciente tiene una enfermedad muy avanzada y requiere tomas de LD frecuentes o va a estar a dieta absoluta durante más de 12-24 horas, se deben considerar tratamientos alternativos a la vía No solo porque el cese abrupto del tratamiento antiparkinsoniano durante más de 24 horas puede ser potencialmente mortal, ya que se puede desencadenar un síndrome de parkinsonismo-hiperpirexia, como se ha descrito previamente (sus síntomas principales son fiebre, disautonomía, alteración del nivel de consciencia o confusión, acinesia, rigidez y elevación de CK), sino para permitir la mejor movilidad y comodidad del paciente. Si el paciente tiene una enfermedad leve-moderada, la mejor opción es la rotigotina, un agonista dopaminérgico que tiene un formato de parche transdérmico de 24 horas de duración. Se debe calcular la dosis que precisa el paciente según las equivalencias conocidas33 (ver calculadora de equivalentes de LD en Pág. 375). Se debe vigilar la aparición de efectos secundarios frecuentes como el eccema cutáneo en la región del parche, náuseas y somnolencia33 (NE-IV).
-
Si el paciente tiene una enfermedad más avanzada, requiere altas dosis de LD (más de 1000 mg) o va a precisar dieta absoluta de forma prolongada, se puede considerar un tratamiento alternativo con apomorfina en perfusión continua. Este agonista dopaminérgico tiene un perfil de actividad similar a la LD (actúa sobre los receptores D1/D2) y puede pautarse en forma de perfusión subcutánea calculando las dosis (ver calculadora de equivalentes de LD en Pág. 375). Este cambio se debe prever con tiempo, ya que la apomorfina puede causar náuseas y vómitos que son evitables con premedicación (domperidona a dosis de 10 mg en desayuno, comida y cena desde 3 días antes). Se debe hacer el cambio de la medicación oral a la perfusión subcutánea la semana previa a la cirugía para optimizar el control de los síntomas y vigilar la posible aparición de hipotensión, somnolencia o ataques de sueño33 (NE-IV).
Manejo intraoperatorio31,32 (NE-IV)
-
El propofol es el fármaco de elección. Puede mejorar el parkinsonismo, pero también inducir discinesias.
-
Se debe evitar la ketamina porque puede provocar una respuesta simpática Se debe evitar el tiopental porque puede reducir la liberación de dopamina a nivel estriatal.
-
Se debe evitar el halotano porque puede interaccionar con la LD y aumentar la sensibilidad cardiaca a las catecolaminas.
-
Los relajantes musculares no despolarizantes son seguros y el rocuronio es de elección.
-
Se deben evitar fármacos con efectos serotoninérgicos en pacientes que toman IMAO (si no se han podido suspender en las semanas previas), ya que la interacción puede producir agitación, rigidez, diaforesis, hiperpirexia e incluso un síndrome serotoninérgico y de manera infrecuente la Algunos opioides con actividad inhibitoria sobre la recaptación de serotonina son la meperidina y en menor medida el tramadol, la metadona, el dextrometorfano y el propoxifeno. Los opioides más seguros son la morfina a dosis bajas, la codeína, la oxicodona y la buprenorfina. A su vez, los IMAO inhiben el metabolismo hepático de los narcóticos, por lo cual se debe ajustar la dosis.
-
En el manejo del dolor, los opioides, y en particular el fentanilo, pueden empeorar la Si el origen del dolor es la rigidez parkinsoniana el mejor tratamiento será el propio de la enfermedad.
-
Los neurolépticos como las fenotiacinas, las butirofenonas y la metoclopramida pueden empeorar la EP y por tanto no deben emplearse nunca en estos pacientes.
-
La indicación de intubación es más frecuente en pacientes con EP que en la población de edad similar porque la disfagia y la bradicinesia de la musculatura respiratoria les hace especialmente vulnerables a sufrir neumonías por broncoaspiración.
-
Si el paciente fuera portador de un neuroestimulador, es recomendable apagar el estimulador durante el procedimiento quirúrgico porque puede interferir con el bisturí eléctrico. Si se debe electrocauterizar, se recomienda la cauterización bipolar.
Manejo posoperatorio
-
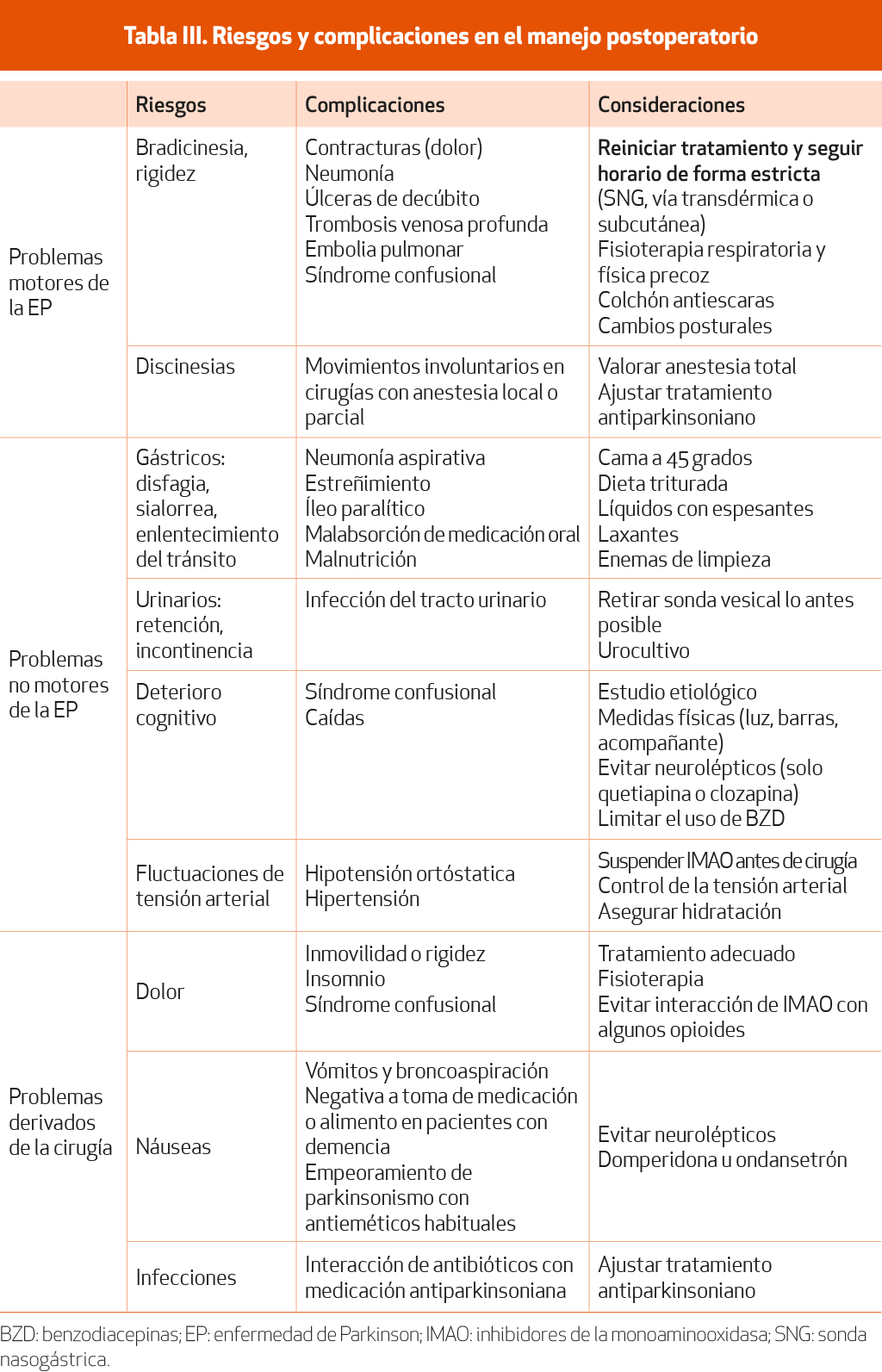
La mayoría de las complicaciones perioperatorias de los pacientes con EP ocurren durante el posoperatorio. Por su enfermedad basal, estos pacientes tienen mayor riesgo de presentar alteraciones motoras, disautonómicas y cognitivas. Los problemas posquirúrgicos más frecuentes son las infecciones (del tracto urinario, de la herida quirúrgica o pulmonares), el síndrome confusional, la hipotensión, las caídas y el mal control de la EP. Se deben anticipar estas complicaciones y considerar aspectos particulares del enfermo parkinsoniano para su mejor manejo (Tabla III)32 (NE-IV).
-
Como se ha señalado con anterioridad, es prioritario que el paciente reciba su medicación antiparkinsoniana lo antes posible tras la cirugía. Para ello, se debe evaluar periódicamente su nivel de consciencia y su capacidad de ingesta oral. Si la vía oral no es posible en las primeras horas del posoperatorio, se debe valorar el poner una sonda nasogástrica para medicación o administrar la medicación antiparkinsoniana por vía transdérmica o subcutánea31 (NE-IV).
-
Se debe comenzar la fisioterapia respiratoria de forma precoz para evitar infecciones respiratorias, la inmovilidad, las contracturas, las trombosis y el estreñimiento31 (NE-IV).
-
El síndrome confusional es frecuente, incluso en pacientes sin deterioro cognitivo previo, y puede ocurrir de forma diferida tras 36 horas de la cirugía en hasta un 70% de los pacientes33. Generalmente se trata de un cuadro de alteración del ritmo sueño-vigilia, acompañado de alucinaciones o delirio y agitación. Como en todo paciente, se debe hacer un estudio para detectar la posible causa (alteraciones metabólicas, infecciones intercurrentes o interacciones medicamentosas). En su manejo son importantes las medidas no farmacológicas (entrada de luz natural, reloj visible, acompañamiento de familiares) y se deben evitar los neurolépticos típicos (haloperidol) y la mayoría de los atípicos (risperidona, olanzapina, aripriprazol, ziprasidona). El uso de estos fármacos empeora el pronóstico de estos pacientes30. En la práctica general, el neuroléptico más utilizado es la quetiapina, porque tiene poco efecto sobre el receptor D2 y por tanto no agrava el parkinsonismo y no precisa monitorización. Sin embargo, si pese a dosis altas (200 mg) no se controla el cuadro confusional, se debe recurrir a la clozapina, ya que es el único fármaco que verdaderamente ha demostrado eficacia en el control de los síntomas psicóticos34 (NE-IV). La agranulocitosis como posible efecto secundario es muy poco frecuente (0,38%) y en el contexto hospitalario la realización de hemogramas seriados semanales las primeras 18 semanas y mensuales después es relativamente En el uso de ambos fármacos se deben tener en cuenta sus posibles efectos secundarios, fundamentalmente la hipotensión y la somnolencia. Se pueden utilizar benzodiacepinas para el insomnio a dosis bajas teniendo en cuenta la posibilidad de depresión respiratoria secundaria31 (NE-IV).

Bibliografía
30. Fung VSC, Aldred J, Arroyo MP, et al. Continuous subcutaneous foslevodopa/foscarbidopa infusion for the treatment of motor fluctuations in Parkinson’s disease: Considerations for initiation and maintenance. Clin Park Relat Disord. 2024;10:100239.
31. Mariscal A, Medrano IH, Alonso-Cánovas A, et al. Manejo perioperatorio de la enfermedad de Parkinson. Neurologia. 2012;27:46-50.
32. Katus L, Shtilbans A. Perioperative management of patients with Parkinson’s disease. Am J Med. 2014;127:275-80.
33. Gerlach OH, Winogrodzka A, Weber WE. Clinical problems in the hospitalized Parkinson’s disease patient: systematic review. Mov Disord. 2011;26:197-208.
34. Seppi K, Weintraub D, Coelho M, et al. The Movement Disorder Society Evidence-Based Medicine Review Update: Treatments for the non-motor symptoms of Parkinson’s disease. Mov Disord. 2011;26 Suppl 3:S42-80.