


La OMS define los cuidados paliativos (CP) como un conjunto de medidas de prevención y alivio del sufrimiento para mejorar la calidad de vida de los pacientes y cuidadores que se enfrentan a problemas asociados a enfermedades que amenazan la vida. Estas medidas se implementan por medio de la identificación temprana, la correcta evaluación y tratamiento tanto de los problemas físicos como de los psicosociales y espirituales1,2.
El objetivo fundamental de los CP es mejorar la calidad de vida de los pacientes; para ello la OMS establece una serie de principios1,2(NE-IV):
Aliviar el dolor y otros síntomas mediante el tratamiento adecuado.
Ayudar a la aceptación del proceso de la enfermedad y la muerte, sin acelerarla ni posponerla. El objetivo es el bienestar y la calidad de vida, no la duración de esta.
Fomentar la autonomía del paciente y apoyarlo para vivir tan activamente como le sea posible.
Aliviar el sufrimiento entendido de forma integral, atendiendo a las necesidades físicas, psíquicas, sociales y espirituales del enfermo y su familia, para lo que es necesario un equipo multidisciplinario.
Informar de una manera gradual, completa y verdadera, respetando el derecho a no ser informado.
Garantizar que no sea tratado en contra de su voluntad y respetar el derecho a la participación en la toma de decisiones.
No deben implicar la renuncia a tratamientos curativos y se debe posibilitar la atención en el domicilio como lugar idóneo para los CP si el paciente lo desea.
Existe una creciente necesidad de CP conforme avanza en gravedad la EP, especialmente si se considera: el deterioro funcional progresivo del paciente, la limitada eficacia del tratamiento sobre los síntomas no motores y la sintomatología axial, la incertidumbre que sufre el paciente y cuidadores en torno al pronóstico de la enfermedad, la complejidad de la toma de decisiones, la sobrecarga de los cuidadores y la alta demanda de atención sanitaria en la fase final de la vida3.
Los CP no solo mejoran la calidad de vida de los pacientes con EP, sino que su integración temprana es crucial para el control sintomático y el alivio de la carga del cuidador4,5 (NE-II). Pese a ello, los CP en la EP todavía no están ampliamente implementados en la práctica clínica, debido, en parte, a la ausencia de protocolos específicos y a la escasa formación del neurólogo en los CP3,6 (NE-II).
En este tema se revisamos el concepto de CP y CP avanzados, el acceso a los servicios de CP, las directrices sobre la información a lo largo de la enfermedad, la identificación de necesidades específicas de CP, el manejo de los síntomas principales, cómo realizar y consultar la declaración de voluntades vitales anticipadas (DVVA) o instrucciones previas. En algunas comunidades también puede efectuarse una planificación anticipada de cuidados (PAC)7.
En noviembre de 2024, un grupo de expertos nacionales ha publicado una serie de recomendaciones para el abordaje de los cuidados paliativos en la enfermedad de Parkinson que animamos al lector a consultar de forma complementaria a este capítulo8.
1. Ruiz Fernández E, Aguirre Clavero E, Escamilla Sevilla F. Cuidados paliativos en la enfermedad de Parkinson. En: Escamilla Sevilla F, González Torres V, Moya Molina MÁ (eds.). Recomendaciones de práctica clínica en la enfermedad de Parkinson 2022. Grupo Andaluz de Trastornos del Movimiento (GATM), Sociedad Andaluza de Neurología (SAN). Barcelona: Editorial Glosa; 2022. p. 269-86. Disponible en: https://portal.guiasalud.es/wp-content/uploads/2022/11/gpc_619_recomendaciones_practica_clinica_parkinson_compl.pdf
2. 67.ª Asamblea Mundial de la Salud. Fortalecimiento de los cuidados paliativos como parte del tratamiento integral a lo largo de la vida. En: Organización Mundial de la Salud [Internet]. Disponible en: https://apps.who.int/gb/ebwha/pdf_files/WHA67-REC1/ A67_2014_REC1-sp.pdf?ua=1&ua=1#page=60
3. Álvarez Saúco M, García-Ramos R, Legarda Ramírez I, et al. Palliative care management in patients with Parkinson’s disease and other movement disorders in Spain. National survey of neurologists. Neurologia (Engl Ed). 2024 Jun;39(5):417-425.
4. Kluger BM, Miyasaki J, Katz M, et al. Comparison of Integrated Outpatient Palliative Care With Standard Care in Patients With Parkinson Disease and Related Disorders. JAMA Neurol. 2020 May 1;77(5):551.
5. Veronese S, Gallo G, Valle A, et al. Specialist palliative care improves the quality of life in advanced neurodegenerative disorders: NE-PAL, a pilot randomised controlled study. BMJ Support Palliat Care. 2017 Jun;7(2):164-72.
6. Gutiérrez Zúñiga R, Ródenas Iruela R, Escamilla Sevilla F. Cuidados paliativos en la enfermedad de Parkinson. En: Escamilla Sevilla F, Olivares Romero J (eds.). Recomendaciones de práctica clínica en la enfermedad de Parkinson. Grupo Andaluz de Trastornos del Movimiento (GATM). Sociedad Andaluza de Neurología. Barcelona: Editorial Glosa; 2017. p. 205-216. Disponible en: https://portal.guiasalud.es/wp-content/ uploads/2018/12/GPC_561_Enfermedad_Parkinson.pdf
7. Martín-Rosselló M, Fernández-López A, Sanz-Amores R, et al. Instrumento diagnóstico de la complejidad en cuidados paliativos. Documento de apoyo al PAI Cuidados Paliativos. Sevilla: Consejería de Igualdad, Salud y Políticas Sociales; 2014. Disponible en: https://www.redpal.es/wp-content/uploads/2018/12/IDC-Pal-2014-Complejidad.pdf
8. Álvarez Saúco M, García-Ramos R, Legarda Ramírez I, Carrillo García F, Fernández Bueno J, Martí Martínez S, et al. Cuidados paliativos en enfermedad de Parkinson y otros trastornos del movimiento. Recomendaciones y protocolo de un grupo multidisciplinar de expertos. Neurologia. 2024 Jun;39(5):417-425.
Los CP en la EP deberían comenzar en la fase diagnóstica simultáneamente con los tratamientos curativos, pero adquieren mayor relevancia en las fases finales de la enfermedad. A lo largo de los años de seguimiento neurológico del paciente se realiza una transición gradual hacia los CP, basándose en las necesidades individuales de cada uno1,6.
En general, se podrían establecer una serie de puntos clave en el proceso de CP en la EP1 (NE-IV):
En las primeras etapas, se debe ofrecer información gradual sobre la enfermedad y el pronóstico, las opciones terapéuticas y el impacto global de la De forma individualizada, se podría dar a conocer la posibilidad de hacer una planificación anticipada de los cuidados (PAC).
Durante la evolución se puede informar sobre la posibilidad de realizar una DVVA y sobre los distintos aspectos del final de la vida, antes de que exista un deterioro cognitivo que dificulte o imposibilite la toma de decisiones.
Es necesario identificar los hitos que definen el comienzo de la fase final de la enfermedad y tratar precozmente los síntomas con mayor impacto, incluyendo el sufrimiento psicológico y el cuidado del cuidador.
En la fase final, se aplicarán las medidas recogidas en el PAC o DVVA si las hubiere, así como las consensuadas con el paciente capaz o con sus cuidadores y familiares, con una adecuación terapéutica personalizada que no omita la atención al duelo de los
Es fundamental en todas las etapas conocer los deseos y preferencias del paciente y mantener su autonomía y dignidad mediante la toma de decisiones compartida9.
Se consideran recursos convencionales aquellos de Atención Primaria y atención hospitalaria que den respuesta a los CP básicos. Ambos deben disponer de competencias transversales en la atención al final de la vida y son los encargados de detectar la necesidad de CP. Existen herramientas para identificar pacientes con necesidad de atención paliativa como el instrumento NECPAL CCOMS-ICO©. Se trata de una serie de 14 preguntas de respuesta dicotómica (“sí/no”); la primera de ellas (“¿le sorprendería que este paciente muriese a lo largo del próximo año?”) ha de ser negativa y, al menos, otra respuesta ha de ser positiva (de los dominios 2, 3 o 4) para identificar al enfermo que requiere medidas paliativas mediante esta estrategia10,11.
Los recursos convencionales, habitualmente la Atención Primaria y el neurólogo referente, son los encargados de hacer una valoración holística del paciente (incluida su situación clínica, funcional, cognitiva y sociofamiliar), determinar la situación de fase terminal y establecer un plan de actuación inicial (problemas detectados, objetivos e intervenciones previstas), que debe quedar registrado en la historia clínica y ser revisado de forma periódica9 (Tabla I) (NE-IV).
Se consideran recursos avanzados los equipos multidisciplinares, integrados por profesionales que dan respuesta a las diferentes situaciones de alta complejidad, los cuales deben disponer de competencias específicas en CP. Para calcular el nivel de complejidad existen herramientas como IDC-Pal que determinará el recurso necesario para la atención paliativa del paciente, siendo necesaria la intervención de los “recursos avanzados” en situaciones altamente complejas y, puntualmente, en situaciones complejas12.

1. Ruiz Fernández E, Aguirre Clavero E, Escamilla Sevilla F. Cuidados paliativos en la enfermedad de Parkinson. En: Escamilla Sevilla F, González Torres V, Moya Molina MÁ (eds.). Recomendaciones de práctica clínica en la enfermedad de Parkinson 2022. Grupo Andaluz de Trastornos del Movimiento (GATM), Sociedad Andaluza de Neurología (SAN). Barcelona: Editorial Glosa; 2022. p. 269-86. Disponible en: https://portal.guiasalud.es/wp-content/uploads/2022/11/gpc_619_recomendaciones_practica_clinica_parkinson_compl.pdf
6. Gutiérrez Zúñiga R, Ródenas Iruela R, Escamilla Sevilla F. Cuidados paliativos en la enfermedad de Parkinson. En: Escamilla Sevilla F, Olivares Romero J (eds.). Recomendaciones de práctica clínica en la enfermedad de Parkinson. Grupo Andaluz de Trastornos del Movimiento (GATM). Sociedad Andaluza de Neurología. Barcelona: Editorial Glosa; 2017. p. 205-216. Disponible en: https://portal.guiasalud.es/wp-content/uploads/2018/12/GPC_561_Enfermedad_Parkinson.pdf
9. Taylor LP, Besbris JM, Graf WD, et al. Clinical Guidance in Neuropalliative Care. Neurology. 2022 Mar 8;98(10):409-16.
10. Gómez-Batiste X, Amblàs J, Costa X, et al. Recomendaciones para la atención integral e integrada de personas con enfermedades o condiciones crónicas avanzadas y pronóstico de vida limitado en servicios de salud y sociales: NEPCAL CCOMS-ICO© 3.1. En: Institut Català d’Oncologia [Internet]. Disponible en: https://ico.gencat.cat/web/.content/minisite/ico/professionals/documents/qualy/arxius/INSTRUMENTO-NECPAL-3.1-2017-ESP_Completo-Final.pdf
11. Gómez-Batiste X, Martínez-Muñoz M, Blay C, et al. Identifying patients with chronic conditions in need of palliative care in the general population: development of the NECPAL tool and preliminary prevalence rates in Catalonia. BMJ Support Palliat Care. 2013 Sep;3(3):300-8.
12. Fernández López A, Bergara de la Fuente M, Boceta Osuna J, et al. Cuidados paliativos. Proceso asistencial integrado. Sevilla: Consejería de Salud y Familias; 2019. Disponible en: https://portal.guiasalud.es/wp-content/uploads/2019/07/pa_9_cuidados_paliativos.pdf
La comunicación del diagnóstico, la evolución y el pronóstico debe realizarse de manera personalizada, de un modo empático, buscando proactivamente las ocasiones en las que el paciente esté preparado para recibir esta información. Dialogar en una etapa temprana de la enfermedad sobre las expectativas e incertidumbres puede influir en las decisiones y mejorar la calidad de vida a medida que la enfermedad avanza13 (NE-IV) (Tabla II). Para ello, es necesario que el neurólogo esté capacitado en distintas habilidades comunicativas, que incluyen dar malas noticias, informar y ayudar en el proceso de toma de decisiones, explicar el pronóstico o establecer límites cuando se planteen procedimientos fútiles. Incluso cuando el pronóstico es incierto para el neurólogo, los pacientes valoran positivamente que se les comunique y se discutan estas incertidumbres11 NE-III).

Un problema común es la dificultad que puede encontrar el paciente para gestionar la información, formular preguntas y entender los distintos escenarios que se puedan presentar, tanto en el diagnóstico como a lo largo de la progresión de la enfermedad. Algunos autores proponen seguir una hoja de ruta que guíe el proceso de información para cubrir los distintos dominios que pueden verse vulnerados en la enfermedad (físicos, psicológicos, sociales, espirituales, culturales, éticos y legales)13 (NE-IV) (Tabla III). Otra estrategia consiste en describir los distintos escenarios y sus implicaciones pronósticas más probables para explorar la aceptación de cada uno de estos por parte del paciente y ayudar en la toma de decisiones9 (NE-IV). Es importante atender las necesidades de información del cuidador, así como vigilar la aparición de síntomas relacionados con el agotamiento (burn-out), especialmente, en los últimos momentos de la enfermedad11 (NE-III). Los cuidadores de pacientes tratados en unidades multidisciplinarias de CP sienten menos agotamiento y ansiedad4,6 (NE-II).
La PAC consiste en el registro en la historia clínica del paciente por parte del profesional sanitario responsable de las preferencias, los valores y deseos del paciente ante ciertas situaciones del final de la vida. Deberá ser un proceso voluntario de comunicación y de toma de decisiones con la persona y se realizará, siempre que esta lo permita, en presencia de una persona de su confianza que vaya a ejercer como su representante12 (NE-IV).

A nivel estatal en la mayoría de las comunidades autónomas existe la opción del registro de DVVA donde el paciente puede registrar de forma oficial sus preferencias respecto a estos aspectos. En función de cada comunidad, existe la opción de que solo pueda ser consultado por el médico que atiende al paciente siempre que este no pueda expresarse por sí mismo.
4. Kluger BM, Miyasaki J, Katz M, et al. Comparison of Integrated Outpatient Palliative Care With Standard Care in Patients With Parkinson Disease and Related Disorders. JAMA Neurol. 2020 May 1;77(5):551.
6. Gutiérrez Zúñiga R, Ródenas Iruela R, Escamilla Sevilla F. Cuidados paliativos en la enfermedad de Parkinson. En: Escamilla Sevilla F, Olivares Romero J (eds.). Recomendaciones de práctica clínica en la enfermedad de Parkinson. Grupo Andaluz de Trastornos del Movimiento (GATM). Sociedad Andaluza de Neurología. Barcelona: Editorial Glosa; 2017. p. 205-216. Disponible en: https://portal.guiasalud.es/wp-content/uploads/2018/12/GPC_561_Enfermedad_Parkinson.pdf.
9. Taylor LP, Besbris JM, Graf WD, et al. Clinical Guidance in Neuropalliative Care. Neurology. 2022 Mar 8;98(10):409-16.
11. Gómez-Batiste X, Martínez-Muñoz M, Blay C, et al. Identifying patients with chronic conditions in need of palliative care in the general population: development of the NECPAL tool and preliminary prevalence rates in Catalonia. BMJ Support Palliat Care. 2013 Sep;3(3):300-8.
12. Fernández López A, Bergara de la Fuente M, Boceta Osuna J, et al. Cuidados paliativos. Proceso asistencial integrado. Sevilla: Consejería de Salud y Familias; 2019. Disponible en: https://portal.guiasalud.es/wp-content/uploads/2019/07/pa_9_cuidados_paliativos.pdf
13. Jordan SR, Kluger B, Ayele R, et al. Optimizing future planning in Parkinson disease: suggestions for a comprehensive roadmap from patients and care partners. Ann Palliat Med. 2020 Feb;9(S1):S63-74.
Es importante considerar en todo momento el abordaje paliativo en la EP, incluso, si es necesario en el momento del diagnóstico, siempre desde una perspectiva dinámica, adaptada a las necesidades del paciente en cada etapa de la enfermedad, y adquiriendo mayor protagonismo en fases avanzadas4,5,12 (NE-II). Se considera estar en dicha fase cuando la discapacidad asociada a los síntomas motores no puede controlarse satisfactoriamente con el mejor tratamiento médico o quirúrgico, cuando la gravedad de los síntomas no motores sobrepasa a la de los síntomas motores, o cuando el tratamiento de los síntomas motores se ve comprometido debido a la aparición de síntomas cognitivos o disautonómicos14
Los pacientes y sus familiares serán valorados y seguidos en Atención Primaria u hospitalaria según sean sus necesidades en cada momento, y en caso de mayor complejidad, serán atendidos por unidades de CP de manera multidisciplinaria.
Aunque puedan aplicarse CP en las distintas fases de la EP, los CP protagonizan la etapa de la EP avanzada (EPA) con síntomas refractarios a tratamiento, habitualmente demencia con/sin comorbilidades graves, es decir, pacientes sin autonomía6.
Se ha diseñado una escala específica para la EP (indicadores de la necesidad de cuidados paliativos en la EP de Radboud Indicators for Palliative Care Needs in Parkinson’s Disease [Radboud o RADPAC-PD]) que identifica a los pacientes que necesitan planificar o iniciar CP avanzados e identificar la fase final de la enfermedad15 (NE-IV) (Tabla IV). Esta fase podría predecirse en pacientes con EP por la presencia de cuatro datos clínicos clave: alucinaciones visuales, caídas frecuentes, demencia y el ingreso en una residencia6,16 (NE-III).
La figura del cuidador es clave en su identificación y evaluación de forma precoz. Se han desarrollado escalas específicas, como la escala de resultados paliativos para los síntomas de la enfermedad de Parkinson (Palliative Outcome Scale-Symptons/Parkinson Disease [POS-S/PD])17 (NE-III). Es una adaptación para la EP de la escala de resultados paliativos (Palliative Outcome Scale [POS]), que recoge 20 síntomas, destacando por su relevancia: los problemas para caminar o usar las manos, el dolor, la dificultad para comunicarse, la fatiga, la salivación excesiva, el estreñimiento, el insomnio y las caídas. Otra escala usada con el mismo propósito es la escala para la evaluación de síntomas de Edmonton para la enfermedad de Parkinson (Edmonton Symptom Assessment System Scale for Parkinson Disease [ESAS-PD]), cuya puntuación en la EPA se asemeja a la de los pacientes con cáncer metastásico18 (NE-III).

4. Kluger BM, Miyasaki J, Katz M, et al. Comparison of Integrated Outpatient Palliative Care With Standard Care in Patients With Parkinson Disease and Related Disorders. JAMA Neurol. 2020 May 1;77(5):551.
5. Veronese S, Gallo G, Valle A, et al. Specialist palliative care improves the quality of life in advanced neurodegenerative disorders: NE-PAL, a pilot randomised controlled study. BMJ Support Palliat Care. 2017 Jun;7(2):164-72.
6. Gutiérrez Zúñiga R, Ródenas Iruela R, Escamilla Sevilla F. Cuidados paliativos en la enfermedad de Parkinson. En: Escamilla Sevilla F, Olivares Romero J (eds.). Recomendaciones de práctica clínica en la enfermedad de Parkinson. Grupo Andaluz de Trastornos del Movimiento (GATM). Sociedad Andaluza de Neurología. Barcelona: Editorial Glosa; 2017. p. 205-216. Disponible en: https://portal.guiasalud.es/wp-content/uploads/2018/12/GPC_561_Enfermedad_Parkinson.pdf
12. Fernández López A, Bergara de la Fuente M, Boceta Osuna J, et al. Cuidados paliativos. Proceso asistencial integrado. Sevilla: Consejería de Salud y Familias; 2019. Disponible en: https://portal.guiasalud.es/wp-content/uploads/2019/07/pa_9_cuidados_paliativos.pdf
14. Miyasaki JM. Parkinson’s Disease and Related Disorders. En: Neuropalliative Care. Cham: Springer International Publishing; 2019. p. 59-72.
15. Lennaerts-Kats H, van der Steen JT, Vijftigschild Z, et al. RADPAC-PD: A tool to support healthcare professionals in timely identifying palliative care needs of people with Parkinson’s disease. PLoS One. 2020 Apr 21;15(4):e0230611.
16. Kempster PA, O’Sullivan SS, Holton JL, et al. Relationships between age and late progression of Parkinson’s disease: a clinico-pathological study. Brain. 2010 Jun 1;133(6):1755-62.
17. Saleem TZ, Higginson IJ, Chaudhuri KR, et al. Symptom prevalence, severity and palliative care needs assessment using the Palliative Outcome Scale: A cross-sectional study of patients with Parkinson’s disease and related neurological conditions. Palliat Med. 2013 Sep 3;27(8):722-31.
18. Miyasaki JM, Long J, Mancini D, et al. Palliative care for advanced Parkinson disease: An interdisciplinary clinic and new scale, the ESAS-PD. Parkinsonism Relat Disord. 2012 Dec;18:S6-9.
Se denomina fase terminal a la presencia de una enfermedad avanzada, progresiva e incurable, sin posibilidades razonables de respuesta al tratamiento específico y con un pronóstico de vida limitado. En esta situación terminal concurren síntomas multifactoriales, cambiantes y de intensidad variable, que causan gran impacto emocional en pacientes y familiares, con demanda de atención. En el caso de una enfermedad no oncológica como la EP, vendrá definida también por la presencia de fracaso orgánico y deterioro progresivo irreversible1. En este sentido, el pronóstico vital y la definición de situación terminal en la EP es muy difícil de establecer, y se puede acompañar de gran incertidumbre. Ello es debido a diversos factores, entre los que se encuentran1,19:
Ausencia de modelos predictivos para el pronóstico vital de enfermedades crónicas no oncológicas.
Oscilaciones en la gravedad clínica, que dificultan establecer el inicio de la fase eminentemente paliativa y la información sobre el final de la vida.
Que la atención corre a cargo de múltiples profesionales, con poca formación en el abordaje de la atención paliativa o de la propia EP.
Carencia de recursos y circuitos adecuados para los CP en esta enfermedad, a diferencia de lo que ocurre en los pacientes oncológicos.
Ubicación variada de los pacientes susceptibles: domicilios, residencias, hospitales, centros de larga estancia o sociosanitarios, etc.
Existe un proyecto multicéntrico europeo PD-Pal para profesionales, pacientes y cuidadores para poder ofrecer CP domiciliarios centrados en el paciente basados en el PAC20.
Se recomienda simplificar y optimizar el tratamiento dopaminérgico, reduciendo o suprimiendo los fármacos antiparkinsonianos adyuvantes a la LD, buscando idealmente el uso de LD en monoterapia, ya que es el medicamento con menor riesgo de inducir efectos adversos en relación con su eficacia sobre el control motor. Se recomienda comenzar por la retirada de fármacos anticolinérgicos, para seguir con la amantadina, los IMAO y, posteriormente, se retirarían los agonistas dopaminérgicos (AD) y los ICOMT. Si, pese a ello, persisten las complicaciones con influencia medicamentosa o yatrogénicas (alucinaciones, delirios, disautonomía o hipersomnia), se intentará reducir la dosis de LD en la medida de lo posible14,19 (NE-IV).
Por otro lado, es imprescindible un correcto manejo de la demencia, de otros síntomas refractarios (por ejemplo, disfagia) y de trastornos intercurrentes (Tabla IV). La atención en unidades de CP multidisciplinarias mejora la sobrecarga del cuidador y la calidad de vida de pacientes con síntomas refractarios: deterioro cognitivo, manifestaciones neuropsiquiátricas incluidos la ansiedad, el dolor, la somnolencia, la disautonomía, el estreñimiento e, incluso, los bloqueos de la marcha4,18 (NE-II).
Es el síntoma principal en CP y también uno de los problemas más relevantes en la EP6. Sus causas son diversas, incluidas aquellas no relacionadas con la enfermedad, aunque la más común es la musculoesquelética, de los miembros superiores, por rigidez, inmovilización o posturas anómalas22. Su evaluación es compleja en pacientes con problemas para comunicarse y, a veces, las causas pueden pasar inadvertidas (por ejemplo, el dolor abdominal por estreñimiento o retención urinaria en situaciones de inmovilización). La figura del cuidador principal es crucial para saber interpretar las muestras de dolor del paciente.
Se deberá tratar el dolor independientemente de la causa, y es necesario identificar el tipo (agudo o crónico, nociceptivo o neuropático) y evaluar su intensidad mediante escalas sencillas como la escala visual analógica (EVA). Además de considerar medidas físicas, hay que elegir el tratamiento farmacológico más idóneo siguiendo la escalera analgésica de la OMS23 (NE-IV) según su intensidad:
Primer escalón (EVA: 1-4). Analgésicos no opioides: paracetamol, metamizol o anti-inflamatorios no esteroideos (AINE).
Segundo escalón (EVA: 4-6). Opioides débiles: tramadol o codeína.
Tercer escalón (EVA: 7-10). Opioides potentes: morfina, fentanilo o La dosificación se realiza según el efecto y la tolerancia. El uso de morfina (por vía oral o por vía subcutánea) es de elección en el dolor grave o la disnea. En general, son fármacos bien tolerados y muy eficaces si se utilizan adecuadamente.
Para el dolor neuropático, pueden considerarse la gabapentina, la pregabalina, benzodiacepinas, antidepresivos, etc. El tratamiento deberá reevaluarse periódicamente en función de la respuesta y la tolerancia.
Además del tratamiento farmacológico, la fisioterapia puede mejorar el dolor, al modular sus vías inhibidoras24 (NE-IV).

La disfagia requiere un abordaje interdisciplinar que incluye a familiares y cuidadores e idealmente valoración por foniatría y logopedia, así como de nutricionistas. A medida que progresa, el equipo asistencial abordará las modificaciones de la dieta y la vía de alimentación, pudiendo considerarse la indicación de alimentación y nutrición artificial. No existen recomendaciones específicas sobre la colocación de sonda nasogástrica o realización de gastrostomía endoscópica percutánea (percutaneous endoscopic gastrostomy [PEG]) en la fase terminal de la EP. En general, se recomienda no mantener una sonda nasogástrica enteral más de tres o cuatro semanas; si la necesidad excede ese tiempo, en casos seleccionados, se puede plantear la realización de una PEG. Previamente es necesario establecer con el paciente y su familia unos objetivos coherentes (hidratación, administración de medicación para el confort, etc.), teniendo en cuenta que, en determinados contextos (demencia y edad avanzada), la implantación de una sonda nasogástrica o la PEG no aumentan la supervivencia, pues no evitan las broncoaspiraciones ni mejoran los parámetros nutricionales1,6 (NE-IV).
Los pacientes con la capacidad de toma de decisiones preservada, que hayan dejado constancia en registros (PAC o DVVA), o por medio de decisiones subrogadas (a través de familiares cercanos), pueden rechazar o interrumpir las intervenciones de soporte vital (como la nutrición e hidratación artificiales, la ventilación mecánica, o cualquier tratamiento no paliativo) bajo el principio ético de respeto a la autonomía, permitiendo una muerte natural. En todo caso, debe asegurarse que dicha decisión se toma con pleno conocimiento de sus consecuencias1,9 (NE-IV).
Es frecuente que muchos pacientes en esta fase tengan pautados tratamientos anticolinesterásicos como la rivastigmina14, en ocasiones con intención de control de la sintomatología psicótica, por lo que se recomienda no retirarlos, excepto en situación de fallecimiento inminente14 (NE-IV).
En primer lugar, se recomienda descartar factores precipitantes como procesos infecciosos (habitualmente, infección del tracto urinario o de las vías respiratorias) o causas metabólicas (típicamente, alteraciones electrolíticas, aunque también déficit de vitamina B12 o hipotiroidismo). Posteriormente se debe revisar la pauta de medicación en busca de fármacos que puedan agravar estos síntomas, así como comprobar la adherencia y cumplimiento del tratamiento. Si es preciso iniciar tratamiento con fármacos neurolépticos, se recomiendan aquellos fármacos con menor efecto parkinsonizante, como son la quetiapina, la clozapina (no es recomendable utilizar inicialmente otros neurolépticos en la EP) e, incluso, la pimavanserina, agonista inverso de los receptores 5-HT2A, que aún no está aprobado en España14. No existen neurolépticos parenterales óptimos para los enfermos de Parkinson. En casos excepcionales y ante síntomas incontrolables se puede utilizar la ziprasidona IM25 (NE-IV).
La inmovilidad mantenida puede provocar dolor, favorecer la rigidez y las úlceras por presión. Si el paciente no deambula y está confinado en una cama o sillón, es necesario buscar posiciones adecuadas, se recomienda realizar cambios posturales frecuentes y seguir un programa de fisioterapia adecuado. En pacientes encamados y muy rígidos, son útiles los colchones antiescaras. En contracturas extremas, puede plantearse el tratamiento con toxina botulínica o, incluso, las tenotomías para permitir la higiene6 (NE-IV).
1. Ruiz Fernández E, Aguirre Clavero E, Escamilla Sevilla F. Cuidados paliativos en la enfermedad de Parkinson. En: Escamilla Sevilla F, González Torres V, Moya Molina MÁ (eds.). Recomendaciones de práctica clínica en la enfermedad de Parkinson 2022. Grupo Andaluz de Trastornos del Movimiento (GATM), Sociedad Andaluza de Neurología (SAN). Barcelona: Editorial Glosa; 2022. p. 269-86. Disponible en: https://portal.guiasalud.es/wp-content/ uploads/2022/11/gpc_619_recomendaciones_practica_clinica_parkinson_compl.pdf
4. Kluger BM, Miyasaki J, Katz M, et al. Comparison of Integrated Outpatient Palliative Care With Standard Care in Patients With Parkinson Disease and Related Disorders. JAMA Neurol. 2020 May 1;77(5):551.
6. Gutiérrez Zúñiga R, Ródenas Iruela R, Escamilla Sevilla F. Cuidados paliativos en la enfermedad de Parkinson. En: Escamilla Sevilla F, Olivares Romero J (eds.). Recomendaciones de práctica clínica en la enfermedad de Parkinson. Grupo Andaluz de Trastornos del Movimiento (GATM). Sociedad Andaluza de Neurología. Barcelona: Editorial Glosa; 2017. p. 205-216. Disponible en: https://portal.guiasalud.es/wp-content/ uploads/2018/12/GPC_561_Enfermedad_Parkinson.pdf
9. Taylor LP, Besbris JM, Graf WD, et al. Clinical Guidance in Neuropalliative Care. Neurology. 2022 Mar 8;98(10):409-16.
14. Miyasaki JM. Parkinson’s Disease and Related Disorders. En: Neuropalliative Care. Cham: Springer International Publishing; 2019. p. 59-72.
18. Miyasaki JM, Long J, Mancini D, et al. Palliative care for advanced Parkinson disease: An interdisciplinary clinic and new scale, the ESAS-PD. Parkinsonism Relat Disord. 2012 Dec;18:S6-9.
19. Fernández Rodríguez R, Giménez Muñoz A, Más Sesé G, et al. La identificación del paciente en fase paliativa en distintos procesos neurológicos. En: Guijarro Castro C, García-Ramos García R, Escamilla Sevilla F (eds.). Manual básico de la SEN sobre el final de la vida y la ley de la eutanasia. San Sebastián de los Reyes (Madrid): Ediciones SEN; 2021. p. 7190.
20. Lennaerts-Kats H, Ebenau A, Kanters S, et al. The Effect of a Multidisciplinary Blended Learning Program on Palliative Care Knowledge for Health Care Professionals Involved in the Care for People with Parkinson’s Disease. J Parkinsons Dis. 2022;12(8):2575-84.
21. Alegre Herrera J. Cuidados paliativos en la enfermedad de Parkinson. En: Escamilla Sevilla F, Mínguez Castellanos A (eds.). Recomendaciones de práctica clínica en la enfermedad de Parkinson Grupo Andaluz de Trastornos del Movimiento (GATM) Sociedad Andaluza de Neurología (SAN). Barcelona: Editorial Glosa; 2012. p. 145-52.
22. Wolff M, Fuentes dos Santos A, Amaral EC, et al. Characterization of pain in patients with Parkinson’s disease: a descriptive cross-sectional study. Research, Society and Development. 2020 Oct 10;9(10):e6069109057.
23. Cancer pain relief. En: Organización Mundial de la Salud [Internet]. Disponible en: https:// iris.who.int/handle/10665/43944
24. Qureshi AR, Jamal MK, Rahman E, et al. Non‐pharmacological therapies for pain management in Parkinson’s disease: A systematic review. Acta Neurol Scand. 2021 Aug 13;144(2):115-31.
25. Oechsner M, Korchhounov A. Parenteral ziprasidone: a new atypical neuroleptic for emergency treatment of psychosis in Parkinson’s disease? Hum Psychopharmacol. 2005 Apr;20(3):203-5.
En los últimos momentos, aparece un importante y rápido deterioro del estado general, caracterizado por una mínima o nula ingesta, astenia extrema, bajo nivel de consciencia, aparición de estertores y signos de mala perfusión tisular. La neumonía aspirativa es la principal causa de muerte (45%)6 (NE-III). Otras causas de fallecimiento son la malnutrición, la embolia pulmonar, la enfermedad cerebrovascular o los eventos cardiovasculares6.
Es clave haber planificado con el paciente y la familia el lugar donde tendrá lugar la defunción. A diferencia de otras enfermedades crónicas con un sufrimiento similar, un porcentaje elevado (40-80%) de pacientes con EP fallecen en ámbito hospitalario1,26. En un estudio realizado al respecto, un 47% de los participantes habían fallecido en el hospital; un 23,7%, en su domicilio; y un 25%, en una residencia. Entre los fallecidos en el hospital apenas se habían mantenido conversaciones acerca de la preferencia sobre el lugar del fallecimiento, y solo un 13,6% fueron remitidos a una unidad de CP6,27 (NE-III). Y, al contrario, una PAC y un adecuado reconocimiento de la muerte inminente están asociados a una muerte no hospitalaria28 (NE-IV). El objetivo de los CP en la fase de final de la vida es garantizar la muerte digna y el apoyo a los familiares. Deben retirarse aquellos fármacos innecesarios y se empleará preferentemente la vía subcutánea si la situación clínica lo permite. Si la atención domiciliaria no es posible en condiciones adecuadas, o por claudicación familiar, puede ser necesario el ingreso hospitalario. En cualquier caso, se deben evitar desplazamientos en situación de muerte inminente6,13 (NE-IV).
En ocasiones, puede ser necesaria la sedación paliativa. La sedación paliativa es la disminución intencionada del nivel de consciencia del enfermo mediante la administración de los fármacos adecuados, con el objetivo de evitar sufrimiento intenso causado por uno o más síntomas refractarios. Puede ser continua o intermitente, y su profundidad se gradúa buscando el nivel de sedación mínimo que logre el alivio sintomático. En los últimos días u horas de vida, la sedación se realizará de forma continua y tan profunda como sea necesario para aliviar el sufrimiento. Es recomendable que se lleve a cabo en el lugar en que está siendo atendido el paciente, ya sea en el hospital o en el domicilio, y que sea aplicada por su médico1,29 (NE-IV).
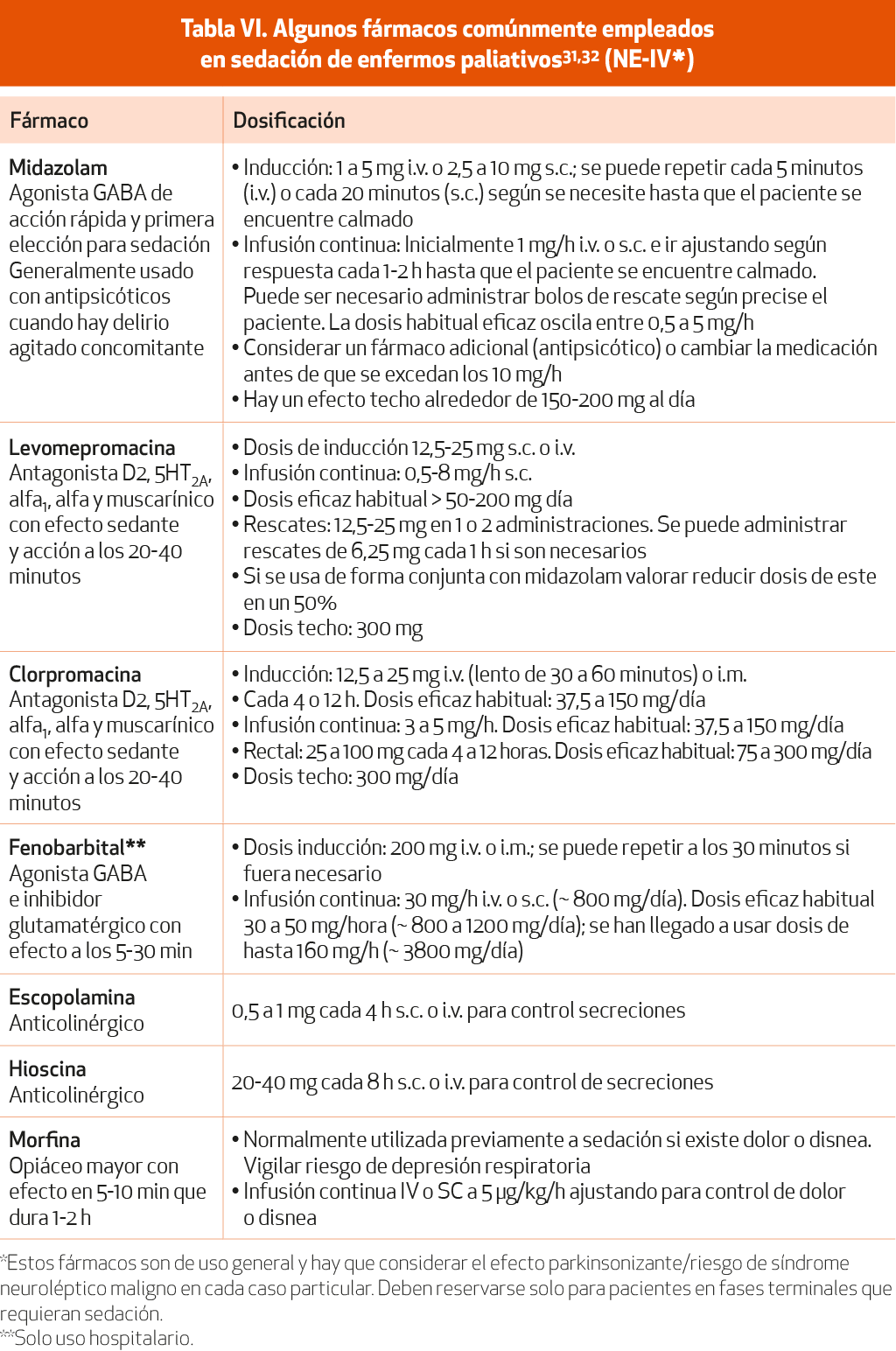
Los fármacos necesarios para un adecuado control de síntomas, así como las medidas de prevención para evitar complicaciones en la fase de agonía, deben mantenerse hasta el final, simplificando al máximo el tratamiento como se ha referido. Son de elección (Tabla VI), por este orden, las benzodiacepinas (midazolam), los neurolépticos sedativos (clorpromazina o levomepromazina), los anticonvulsivos (fenobarbital) y los anestésicos (propofol). El midazolam es siempre la primera opción, excepto si el síntoma refractario es el delirio, siendo en este caso de elección la levomepromazina. La vía de administración de elección es la subcutánea, sobre todo si la venosa no es fácilmente canalizable o si el paciente se encuentra en el domicilio. Puede ser necesaria la administración de otros fármacos: anticolinérgicos (como antisecretores bronquiales) y los opioides, que no deben ser retirados durante la sedación, aunque puede reducirse su dosis1,29 (NE-IV).
Como con cualquier otro tratamiento, se debe realizar una evaluación continua del nivel de sedación en el que se encuentra y necesita el paciente. Se recomienda para este fin la escala de Ramsay30 (Tabla VII). En la historia clínica y en las hojas de evolución, deberán registrarse con el detalle necesario los datos relativos al ajuste de las dosis de los fármacos utilizados, a la evolución clínica de la sedación en la agonía y a los cuidados básicos administrados29.

1. Ruiz Fernández E, Aguirre Clavero E, Escamilla Sevilla F. Cuidados paliativos en la enfermedad de Parkinson. En: Escamilla Sevilla F, González Torres V, Moya Molina MÁ (eds.). Recomendaciones de práctica clínica en la enfermedad de Parkinson 2022. Grupo Andaluz de Trastornos del Movimiento (GATM), Sociedad Andaluza de Neurología (SAN). Barcelona: Editorial Glosa; 2022. p. 269-86. Disponible en: https://portal.guiasalud.es/wp-content/ uploads/2022/11/gpc_619_recomendaciones_practica_clinica_parkinson_compl.pdf
6. Gutiérrez Zúñiga R, Ródenas Iruela R, Escamilla Sevilla F. Cuidados paliativos en la enfermedad de Parkinson. En: Escamilla Sevilla F, Olivares Romero J (eds.). Recomendaciones de práctica clínica en la enfermedad de Parkinson. Grupo Andaluz de Trastornos del Movimiento (GATM). Sociedad Andaluza de Neurología. Barcelona: Editorial Glosa; 2017. p. 205-216. Disponible en: https://portal.guiasalud.es/wp-content/ uploads/2018/12/GPC_561_Enfermedad_Parkinson.pdf
13. Jordan SR, Kluger B, Ayele R, et al. Optimizing future planning in Parkinson disease: suggestions for a comprehensive roadmap from patients and care partners. Ann Palliat Med. 2020 Feb;9(S1):S63-74.
26. Nicholas R, Nicholas E, Hannides M, et al. Influence of individual, illness and environmental factors on place of death among people with neurodegenerative diseases: a retrospective, observational, comparative cohort study. BMJ Support Palliat Care. 2024 May;14(e1):e1032-40.
27. Walker RW, Churm D, Dewhurst F, et al. Palliative care in people with idiopathic Parkinson’s disease who die in hospital: Table 1. BMJ Support Palliat Care. 2014 Mar;4(1):64-7.
28. Nicholas R, Nicholas E, Hannides M, et al. Influence of individual, illness and environmental factors on place of death among people with neurodegenerative diseases: a retrospective, observational, comparative cohort study. BMJ Support Palliat Care. 2024 May;14(e1):e1032–40.
29. Grupo de trabajo de la Guía de Práctica Clínica sobre atención paliativa al adulto en situación de últimos días. Guía de Práctica Clínica sobre atención paliativa al adulto en situación de últimos días. Madrid: Ministerio de Sanidad, Santiago de Compostela: Agencia de Conocimiento en Salud (ACIS). Unidad de Asesoramiento Científico-técnico, Avalia-t; 2021.
30. Ramsay MAE, Savege TM, Simpson BRJ, et al. Controlled sedation with alphaxalone-alphadolone. Br Med J. 1974 Jun 22;2(5920):656–9.
31. OMC, SECPAL. Guía de sedación paliativa. En: Organización Médica Colegial de España [Internet]. Disponible en: https://www.cgcom.es/sites/main/files/mig/guia_sedaccion_ paliativa.pdf
32. Nathan Cherny. Palliative Sedation. En: UpToDate [internet]. Disponible en: https:// www.uptodate.com/contents/palliative-sedation
El 24 de marzo de 2021 se publicó en el Boletín Oficial del Estado la ley orgánica que regula la Eutanasia en España33 y cuyo objeto literalmente es:
El objeto de esta Ley es regular el derecho que corresponde a toda persona que cumpla las condiciones exigidas a solicitar y recibir la ayuda necesaria para morir, el procedimiento que ha de seguirse y las garantías que han de observarse. Asimismo, determina los deberes del personal sanitario que atienda a esas personas, definiendo su marco de actuación, y regula las obligaciones de las administraciones e instituciones concernidas para asegurar el correcto ejercicio del derecho reconocido en esta Ley”.
Los requisitos literales para poder solicitar la ayuda a morir según la ley son:
1. Para poder recibir la prestación de ayuda para morir será necesario que la persona cumpla todos los siguientes requisitos:
Tener la nacionalidad española o residencia legal en España o certificado de empadronamiento que acredite un tiempo de permanencia en territorio español superior a doce meses, tener mayoría de edad y ser capaz y consciente en el momento de la solicitud.
Disponer por escrito de la información que exista sobre su proceso médico, las diferentes alternativas y posibilidades de actuación, incluida la de acceder a cuidados paliativos integrales comprendidos en la cartera común de servicios y a las prestaciones que tuviera derecho de conformidad a la normativa de atención a la dependencia.
Haber formulado dos solicitudes de manera voluntaria y por escrito, o por otro medio que permita dejar constancia, y que no sea el resultado de ninguna presión externa, dejando una separación de al menos quince días naturales entre ambas.
Si el médico responsable considera que la pérdida de la capacidad de la persona solicitante para otorgar el consentimiento informado es inminente, podrá aceptar cualquier periodo menor que considere apropiado en función de las circunstancias clínicas concurrentes, de las que deberá dejar constancia en la historia clínica.
Sufrir una enfermedad grave e incurable o un padecimiento grave, crónico e imposibilitante en los términos establecidos en esta Ley, certificada por el médico responsable.
Prestar consentimiento informado previamente a recibir la prestación de ayuda para morir. Dicho consentimiento se incorporará a la historia clínica del paciente.
2. No será de aplicación lo previsto en las letras b), c) y e) del apartado anterior en aquellos casos en los que el médico responsable certifique que el paciente no se encuentra en el pleno uso de sus facultades ni puede prestar su conformidad libre, voluntaria y consciente para realizar las solicitudes, cumpla lo previsto en el apartado d), y haya suscrito con anterioridad un documento de instrucciones previas, testamento vital, voluntades anticipadas o documentos equivalentes legalmente reconocidos, en cuyo caso se podrá facilitar la prestación de ayuda para morir conforme a lo dispuesto en dicho documento. En el caso de haber nombrado representante en ese documento será el interlocutor válido para el médico responsable.
La valoración de la situación de incapacidad de hecho por el médico responsable se hará conforme a los protocolos de actuación que se determinen por el Consejo Interterritorial del Sistema Nacional de Salud.
Es posible por tanto que en algunos supuestos las personas con EP en fases terminales o de situación de irreversibilidad de síntomas incapacitantes, como se recoge en el apartado 1d de dicha ley, puedan demandar esta ayuda. Remitimos al lector a los recursos específicos en cada Comunidad Autónoma para profundizar en este importante aspecto relativo a decisiones del final de la vida, así como índoles de aspecto práctico de cómo implementarlo. Es importante también resaltar que el profesional sanitario tiene derecho a la objeción de conciencia existiendo un registro específico para ello privado y confidencial.

1. Ruiz Fernández E, Aguirre Clavero E, Escamilla Sevilla F. Cuidados paliativos en la enfermedad de Parkinson. En: Escamilla Sevilla F, González Torres V, Moya Molina MÁ (eds.). Recomendaciones de práctica clínica en la enfermedad de Parkinson 2022. Grupo Andaluz de Trastornos del Movimiento (GATM), Sociedad Andaluza de Neurología (SAN). Barcelona: Editorial Glosa; 2022. p. 269-86. Disponible en: https://portal.guiasalud.es/wp-content/ uploads/2022/11/gpc_619_recomendaciones_practica_clinica_parkinson_compl.pdf
33. Ley Orgánica 3/2021, de 24 de marzo, de regulación de la eutanasia. En: Boletín Oficial del Estado [Internet]. Disponible en: https://www.boe.es/eli/es/lo/2021/03/24/3


