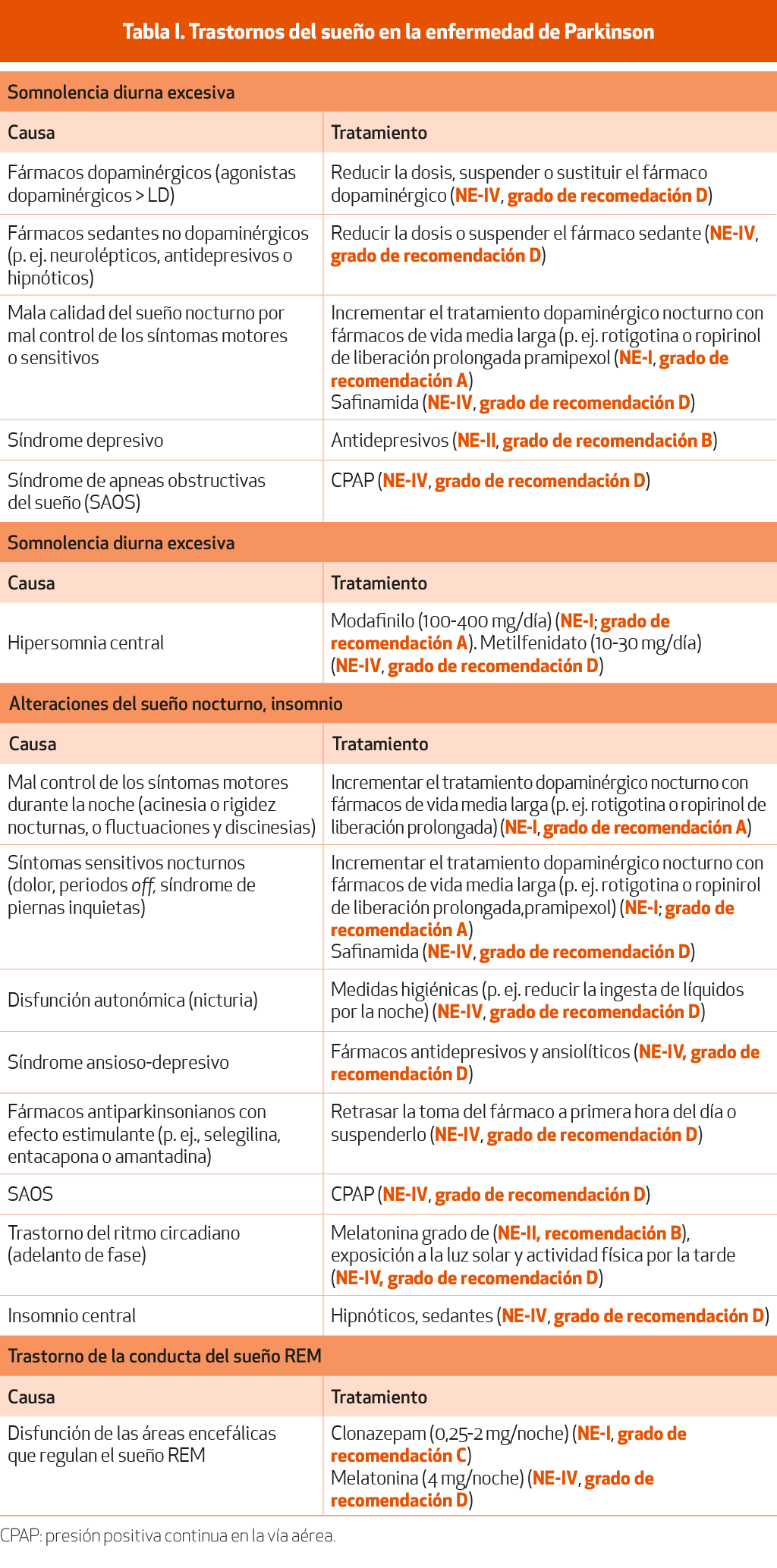
Los trastornos del sueño incluyen la somnolencia diurna excesiva (SDE), las alteraciones del sueño nocturno con el insomnio y el trastorno de conducta durante el sueño REM (TCSR) (Tabla I). Estos trastornos del sueño son especialmente frecuentes en la EP avanzada, probablemente debido a la combinación de diversos factores, como por ejemplo el incremento en el tratamiento dopaminérgico y el uso de otros fármacos, el empeoramiento de los síntomas motores de la enfermedad y, quizás, la neurodegeneración de las áreas encefálicas que regulan la vigilia y el sueño. Una excepción sería el TCSR, que con frecuencia antecede a los síntomas motores de la enfermedad o puede estar ya presente en el momento del diagnóstico de la EP.
Somnolencia diurna excesiva
Puede afectar a entre un 12 y un 84% de los pacientes. En un 0,5-20% de ellos, la SDE se puede presentar en la forma de episodios súbitos de sueño irresistible o ataques de sueño1.
Las causas de somnolencia en la EP pueden ser diversas. La SDE puede ser un efecto secundario de los fármacos dopaminérgicos, incluyendo la LD, pero en especial de todos los agonistas dopaminérgicos. En algunos pacientes la relación entre la SDE y los fármacos dopaminérgicos es clara, pues la somnolencia aparece al introducir o incrementar la dosis del fármaco. Otra causa de SDE en la EP puede ser la administración como consecuencia de comorbilidades neuropsiquiátricas de otros fármacos con efecto sedante, como por ejemplo neurolépticos, antidepresivos o hipnóticos. Un insomnio y un sueño nocturno insuficiente por los problemas asociados a un mal control de los síntomas motores o sensitivos por la noche también pueden dar lugar a SDE. La SDE en la EP también puede estar en relación con la presencia de una depresión, otro síntoma no motor frecuente en la EP. Si bien el SAOS no ocurre con más frecuencia en la EP que en la población general, un SAOS coincidental también puede ser la causa de una SDE en un paciente con EP. Finalmente, la SDE puede ser un síntoma propio de la EP, causado por la degeneración de las estructuras encefálicas que promueven la vigilia, incluyendo el hipotálamo y estructuras del tronco como el locus coeruleus, el área dopaminérgica ventral-tegmental mesencefálica, el núcleo pedunculopontino o los núcleos del rafe. Así pues, el tratamiento de la somnolencia en la EP dependerá de la causa, y es importante considerar que en un mismo paciente pueden coexistir varias de ellas.
En cuanto al tratamiento, el primer paso será alertar al paciente sobre la peligrosidad de conducir o realizar otras actividades de riesgo hasta que la somnolencia no se resuelva. El siguiente paso será evaluar si la somnolencia puede tener una causa farmacológica. Si está en relación con algún fármaco dopaminérgico, se puede considerar reducir la dosis o incluso suspender el fármaco, o bien cambiar a otro medicamento dopaminérgico2,3 (NE-IV), si bien todo ello puede comportar un empeoramiento de los síntomas motores. Si existe alguna medicación no dopaminérgica sedante, se debe valorar la posibilidad de suprimirla o disminuir la dosis4 (NE-IV). Si no existe una causa farmacológica, se deberá considerar si hay un mal control de los síntomas motores o sensitivos nocturnos que puedan causar un sueño nocturno insuficiente, y si es preciso optimizar el tratamiento antiparkinsoniano por la noche evitando dosis elevadas antes de dormir y usar formulaciones retard, aunque hay resultados contradictorios5 (NE-IV). Si existe una depresión, se deberá tratar adecuadamente6 (NE-I). Por otro lado, se debe preguntar, sobre todo al cónyuge o al cuidador del paciente, por la presencia de ronquidos y apneas, y si se sospecha un SAOS, realizar un polisomnograma. Si se confirma un índice elevado de apneas obstructivas, estará indicado realizar una prueba terapéutica con presión positiva continua en la vía aérea (CPAP)7 (NE-IV). Cuando no exista ninguna causa evidente y se considere que la SDE puede ser un síntoma propio de la EP, se puede valorar realizar una prueba con fármacos estimulantes como el modafinilo (entre 100 y 400 mg al día) (existen tres estudios con NE-I: en dos se sugiere que es un tratamiento eficaz para la somnolencia en la EP y en el otro que es ineficaz)8-10.
Alteraciones del sueño nocturno
Hasta un 55% de los pacientes con EP presentan sueño fragmentado y despertar precoz, que son los tipos de insomnio más frecuentes11. El insomnio en la EP también puede tener diferentes causas, pudiendo estar en relación con los síntomas motores y no motores de la enfermedad u otros factores. Un mal control de los síntomas motores durante la noche, como la presencia de acinesia o rigidez, así como de fluctuaciones o discinesias, podría despertar al paciente y causar un sueño fragmentado. Por otro lado, la existencia de síntomas sensitivos nocturnos, como dolor por la rigidez, por la imposibilidad de cambiar de postura, o dolor en relación con los periodos off, o bien la presencia de un síndrome de piernas inquietas, también pueden fragmentar el sueño. Una disfunción autonómica como la nicturia, la depresión o la ansiedad son otras causas de una mala calidad y fragmentación del sueño. Además, fármacos antiparkinsonianos como la selegilina, la amantadina o la entacapona pueden alertar excesivamente al paciente durante la noche12 (NE-IV).
Otros fármacos también utilizados en el tratamiento de estos pacientes, como anticolinesterásicos, ISRS o venlafaxina también pueden aumentar el insomnio12. Por otro lado, en los pacientes con EP pueden coexistir otros trastornos del sueño que son frecuentes en las personas de edad avanzada y que pueden fragmentar el sueño y causar un despertar precoz, como serían el SAOS o un trastorno del ritmo circadiano en la forma de un adelanto de fase. Finalmente, el insomnio también podría ser un síntoma propio de la EP, causado por la degeneración de las estructuras encefálicas que regulan la vigilia y el sueño. Establecer cuál de todos estos factores es el responsable de la alteración del sueño nocturno en un paciente con EP puede ser difícil.
Medidas específicas (dependerá de las causas) para tratar el insomnio en la EP incluyen la supresión de la selegilina o la amantadina cuando se administran por la tarde o por la noche13 (NE-II) o, cuando hay síntomas motores o sensitivos nocturnos significativos, optimizar el tratamiento antiparkinsoniano con la administración de agentes dopaminérgicos de vida media larga o de liberación sostenida como la rotigotina o el ropirinol de liberación prologada, que pueden ser útiles para evitar los periodos off durante la noche14-15 (NE-I). Si el paciente presenta un síndrome de piernas inquietas asociado, el uso de agentes dopaminérgicos de larga duración o, en su caso, fármacos como la gabapentina podría ser de utilidad16 (NE-II). En el caso de existir una depresión o un síndrome ansioso, deben ser tratados de forma correcta17 (NE-IV).
Otros fármacos, como la safinamida, han mostrado un efecto beneficioso en el sueño nocturno y sobre la somnolencia diurna18-20 (NE-IV).
La estimulación cerebral profunda del núcleo subtalámico y los tratamientos de perfusión como la apomorfina subcutánea y LD/carbidopa intestinal mejoran la calidad del sueño, aunque no están indicadas con este objetivo21 (NE-III).
Trastorno de la conducta del sueño REM
Caracterizado por la presencia de pesadillas y conductas violentas durante el sueño REM, está presente entre un 23 y un 58% de los pacientes con EP22. La fisiopatología de esta parasomnia en la EP está en relación con la degeneración de las áreas del tronco encefálico que modulan el sueño REM. El clonazepam es el fármaco más utilizado en dosis única de 0,5 a 2 mg antes de acostarse, con una alta tasa de respuesta en distintas series23 (NE-I).
Cuando el clonazepam no es eficaz, una posible alternativa sería la melatonina 4 mg 2 horas antes de acostarse24 (NE-IV). Siempre es importante considerar la posibilidad de otro trastorno de sueño diferente al TCSR como la causa de las conductas anormales durante el sueño, como por ejemplo un SAOS, sobre todo si el clonazepam se muestra ineficaz y agrava las conductas anormales, y en especial si hay antecedentes de ronquidos y apneas observadas. En tal caso estaría indicado realizar un videopolisomnograma para confirmar el diagnóstico de un TCSR o descartar un SAOS, que por otro lado podría ser agravado por el tratamiento con clonazepam.
Bibliografía
1. Ondo WG, Dat Vuong K, Khan H, et al. Daytime sleepiness and other sleep disorders in Parkinson’s disease. Neurology. 2001;57:1392-1396.
2. Razmy A, Lang AE, Shapiro CM. Predictors of impaired daytime sleep and wakefulness in patients with Parkinson disease treated with older (ergot) vs newer (nonergot) dopamine agonists. Arch Neurol. 2004;61:97-102.
3. Pal S, Bhattacharya KF, Agapito C, et al. A study of excessive daytime sleepiness and its clinical significance in three groups of Parkinson’s disease patients taking pramipexole, cabergoline and levodopa mono and combination therapy. J Neural Transm 2001;108:71–77.
4. Martins Rodrigues T, Castro Caldas A, Ferreira JJ. Pharmacological interventions for daytime sleepiness and sleep disorders in Parkinson’s disease: systematic review and meta-analysis. Parkinsonism Relat Disord. 2016;27:25-34.
5. Chahine LM, Daley J, Horn S, et al. Association between dopaminergic medications and nocturnal sleep in early-stage Parkinson’s disease. Parkinsonism Relat Disord. 2013 Oct;19(10):859-63.
6. Menza M, Dobkin RD, Marín H, et al. A controlled trial of antidepressants in patients with Parkinson disease and depression. Neurology. 2009 Mar 10;72(10):886-92.
7. Neikrug AB, Liu L, Avanzino JA, et al. Continuous positive airway pressure improves sleep and daytime sleepiness in patients with Parkinson disease and sleep apnea. Sleep. 2014;37(1):177-185.
8. Adler CH, Caviness JN, Hentz JG, et al. Randomized trial of modafinil for treating subjective daytime sleepiness in patients with Parkinson’s disease. Mov Disord. 2003;18:287-93.
9. Högl B, Saletu M, Brandauer E, et al. Modafinil for the treatment of daytime sleepiness in Parkinson’s disease: a double-blind, randomized, crossover, placebo-controlled polygraphic trial. Sleep. 2002;25:905-9.
10. Ondo WG, Fayle R, Atassi F, et al. Modafinil for daytime somnolence in Parkinson’s disease: double blind, placebo controlled parallel trial. J Neurol Neurosurg Psychiatry. 2005;76:1636-9.
11. Dodet P, Houot M, Leu-Semenescu S, et al. Sleep disorders in Parkinson’s disease, an early and multiple problem. NPJ Parkinsons Dis. 2024 Feb 29;10(1):46.
12. Taximaimaiti R, Luo X, Wang XP. Pharmacological and non-pharmacological treatments of sleep disorders in Parkinson’s disease. Curr Neuropharmacol. 2021;19(12):2233-49.
13. Fahn S, Isgreen WP. Long-term evaluation of amantadine and levodopa combination in parkinsonism by double-blind corssover analyses. Neurology. 1975 Aug;25(8):695-700.
14. Pahwa R, Stacy MA, Factor SA, et al. Ropinirole 24-hour prolonged release: randomized, controlled study in advanced Parkinson disease. Neurology. 2007;68:1108-15.
15. Trenkwalder C, Kies B, Rudzinska M, et al. Rotigotine effects on early morning motor function and sleep in Parkinson’s disease: a double-blind, randomized, placebo-controlled study (RECOVER). Mov Disord. 2011;26:90-9.
16. García-Borreguero D, Larrosa O, de la Llave Y, et al. Treatment of restless legs syndrome with gabapentin: a double-blind, cross-over study. Neurology. 2002 Nov 26;59(10):1573-9.
17. Kay DB, Tanner JJ, Bowers D. Sleep disturbances and depression severity in patients with Parkinson’s disease. Brain Behav. 2018 Jun;8(6):e00967.
18. Santos García D, Cabo López I, Labandeira Guerra C, et al. Safinamide improves sleep and daytime sleepiness in Parkinson’s disease: results fromthe SAFINONMOTOR study. Neurol Sci. 2022;43(4):2537-44.
19. Bianchi MLE, Riboldazzi G, Mauri M, et al. Efficacy of safinamide on non-motor symptoms in a cohort of patients affected by idiopathic Parkinson’s disease. Neurol Sci. 2019;40(2):275-279.
20. Liguori C, Stefani A, Runi R, et al. Safinamide effect on sleep disturbances and daytime sleepiness in motor fluctuating Parkinson’s disease patients: A validated questionnaires- controlled study. Park Relat Disord. 2018;57:80-81.
21. Zibetti M, Romagnolo A, Merola A, et al. A polysomnographic study in parkinsonian patients treated with intestinal levodopa infusion. J Neurol. 2017 Jun;264(6):1085-1090.
22. Zhang J, Xu CY, Liu J. (2017). Meta-analysis on the prevalence of REM sleep behavior disorder symptoms in Parkinson’s disease. BMC Neurol. 2017;17(1):23.
23. Shin C, Park H, Lee WW, et al. Clonazepam for probable REM sleep behavior disorder in Parkinson’s disease: A randomized placebo-controlled trial. J Neurol Sci. 2019 Jun 15;401:81-86.
24. Byun JI, Shin YY, Seong YA, et al. Comparative efficacy of prolonged-release melatonin versus clonazepam for isolated rapid eye movement sleep behavior disorder. Sleep Breath. 2023 Mar;27(1):309-318.